A. Pembuatan Asid Nitrik
- Terdapat banyak kegunaan ammonia. Satu ☝ daripada kegunaan ammonia ialah untuk membuat asid nitrik melalui Proses Ostwald.
- Penghasilan asid nitrik memerlukan keadaan yang berikut 👉 :
- Suhu : 800°C 🔥
- Tekanan : 10 atmosfera
- Mangkin : Platinum
B. Pembuatan Ammonia
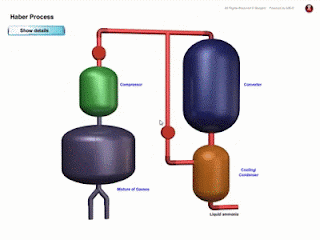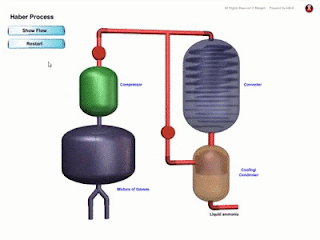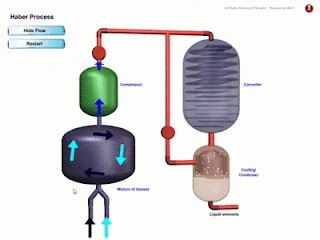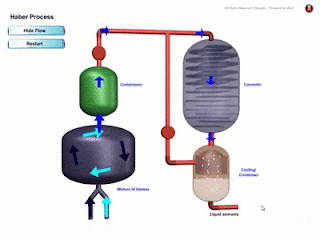
- Ammonia NH3 dihasilkan dalam industri melalui Proses Haber.
- Bahan-bahan mentah untuk penghasilan ammonia, NH3 ialah gas nitrogen H2 dan gas oksigen, O2.
- Gas nitrogen, N2 diperoleh daripada penyulingan berperingkat ke atas udara cecair.
- Gas hidrogen, H2 diperoleh daripada gas asli.
- Dalam penghasilan ammonia, NH3, gas nitrogen, N2 dan gas hidrogen, H2 dicampurkan mengikut nisbah isi padu 1 N2 : 3 H2 ke dalam pemampat. Persamaan Kimia : N2 (g) + 3H2 (g) ⇌ 2NH3 (g)
- Penghasilan ammonia,NH3, memerlukan keadaan yang berikut 👉 :
- Suhu : 450°C 🔥
- Tekanan : 200 atmosfera
- Mangkin : Besi
C. Kegunaan Ammonia
Ammonia yang berformula NH3 ialah sebatian yang sangat berguna 😄 dalam industri. Contohnya :
- Membuat baja bernitrogen 🌳 dalam bentuk ammonium sulfat, ammonium nitrat dan urea.
- Dalam bentuk cecair, ammonia digunakan sebagai bahan penyejuk dalam peti sejuk.
- Sebagai bahan mentah untuk pembuatan asid nitrik dalam Proses Ostwald.
- Ditukarkan kepada asid nitrik untuk digunakan dalam pembuatan bahan letupan 💣.
- Sebagai alkali untuk mencegah ❌ pengumpulan susu getah apabila susu getah perlu disimpan dalam bentuk cecair.
- Menghasilkan ammonium klorida yang digunakan dalam pembuatan sel kering.

D. Penyediaan Baja Ammonium
- Baja ammonium 🌱 ialah baja bernitrogen yang dapat membekalkan unsur nitrogen untuk tumbuhan.
- Baja-baja ammonium dihasilkan melalui tindak balas peneutralan antara larutan ammonia NH3 dengan larutan asid.
- Baja berlainan mengandungi peratusan nitrogen mengikut jisim yang berbeza.
- Peratusan nitrogen mengikut jisim boleh dihitung dengan menggunakan rumus berikut : (Jisim nitrogen / Jisim molekul relatif baja) x 100%
1. Urea, CO(NH2)2
- Tindak balas peneutralan : Larutan Ammonia + Karbon Dioksida
- Persamaan Kimia : 2NH3 (g) + CO2 (g) ➝ CO(NH2) (p) + H2O (ce)
- ( 2(14) / (12 + 16 + 2(14) + 4(1) ) ) x 100 % = 46.7%
- Mengandungi 46.7% nitrogen 😲

 2. Ammonium Nitrat, NH4NO3
2. Ammonium Nitrat, NH4NO3
- Tindak balas peneutralan : Larutan Ammonia + Asid Nitrik
- Persamaan Kimia : NH3 (ak) + HNO3 (ak) ➝ NH4NO3 (ak)
- ( 2(14) / (2(14) + 4(1) + 3(16)) ) x 100 % = 35%
- Mengandungi 35% nitrogen 😯
 3. Ammonium Sulfat, (NH4)2SO4
3. Ammonium Sulfat, (NH4)2SO4
- Tindak balas peneutralan : Larutan Ammonia + Asid Sulfurik
- Persamaan Kimia : 2NH3 (ak) + H2SO4 (ak) ➝ (NH4)2SO4 (ak)
- ( 2 (14) / ( 2(14) + 8(1) + 32 + 16(4)) ) x 100 % = 21.2%
- Mengandungi 21.2% nitrogen 😮
Baja yang mengandungi lebih banyak nitrogen adalah lebih baik. Daripada kiraan di atas, ianya menunjukkan bahawa baja Urea, CO(NH2)2 adalah baja yang terbaik 😱 antara ketiga-tiga baja tersebut ❗

The best
BalasPadamThank youu!
Padamthankyouu
BalasPadamu're welc!
Padam